Het Europees Comité voor geneesmiddelen voor menselijk gebruik (CHMP) heeft een positieve aanbeveling gedaan voor nivolumab als monotherapie voor de behandeling van plaveiselcelcarcinoom van het hoofd-halsgebied (SCCHN) bij volwassen patiënten met ziekteprogressie tijdens of na op platina gebaseerde chemotherapie.
Het Europees Comité voor geneesmiddelen voor menselijk gebruik (CHMP) heeft een positieve aanbeveling gedaan voor nivolumab als monotherapie voor de behandeling van plaveiselcelcarcinoom van het hoofd-halsgebied (SCCHN) bij volwassen patiënten met ziekteprogressie tijdens of na op platina gebaseerde chemotherapie. De aanbeveling van het CHMP zal worden geverifieerd door de Europese Commissie (EC), die beslist over de goedkeuring van geneesmiddelen voor gebruik in de Europese Unie. Dit is de eerste positieve aanbeveling van het CHMP voor een PD-1-remmer bij dit type behandeling van plaveiselcelcarcinoom van het hoofd-halsgebied. Tot nu toe is nivolumab door de Europese Commissie goedgekeurd voor zes indicaties voor de behandeling van vier verschillende soorten kanker.
"Bijna de helft van alle patiënten met plaveiselcelcarcinoom van het hoofd-halsgebied zal binnen twee jaar na stopzetting van de behandeling een terugval ervaren, en er is slechts een bescheiden verbetering van de behandelresultaten in de afgelopen 10 jaar, wat aangeeft dat er dringend nieuwe behandelingsopties moeten worden gevonden voor patiënten met deze slopende ziekte." , zegt Emmanuel Blin, Senior Vice President en Chief Strategic Officer van Bristol-Myers Squibb. “We zijn erg blij dat het Comité voor geneesmiddelen voor menselijk gebruik (CHMP) de registratie van nivolumab heeft aanbevolen voor de behandeling van volwassen patiënten met plaveiselcelkanker van het hoofd-halsgebied die progressie hebben geboekt tijdens of na op platina gebaseerde chemotherapie. We zullen samenwerken met de Europese Commissie om deze behandeling te beoordelen als een mogelijke therapeutische optie voor patiënten in de Europese Unie. "
Het Europees Comité voor geneesmiddelen voor menselijk gebruik (CHMP) heeft een gunstig advies uitgebracht op basis van de resultaten van een centrale, open-label, gerandomiseerde fase 3-klinische studie waarin de algehele overleving (OS) van behandeling met nivolumab werd beoordeeld bij eerder behandelde patiënten met post-chemotherapie plaveisel hoofd-halskanker gebaseerd op platinaverbindingen vergeleken met de keuze van de onderzoeker (methotrexaat, docetaxel of cetuximab) als adjuvante therapie voor primaire, recidiverende of gemetastaseerde tumoren. Op basis van de geplande tussentijdse analyse werd de klinische studie begin januari 2016 afgerond als resultaat van een beoordeling door de onafhankelijke Data Monitoring Committee, waaruit bleek dat de primaire eindpunten, d.w.z. een hogere algehele overleving, werden bereikt bij patiënten die werden behandeld met nivolumab in vergelijking met patiënten die werden behandeld naar keuze van de onderzoeker. De gegevens over de algehele overleving werden voor het eerst gepresenteerd op de jaarvergadering van de American Cancer Research Society in 2016. Het veiligheidsprofiel van nivolumab in de CheckMate -141-studie was consistent met dat verkregen in eerdere klinische onderzoeken met andere kankers.
Informatie over nivolumab
Nivolumab is een PD-1-immuuncontrolepuntremmer die op unieke wijze is ontworpen om het immuunsysteem van het lichaam te helpen een immuunrespons te herstellen. Door het immuunsysteem van het lichaam te ondersteunen om kanker te bestrijden, is nivolumab een belangrijke therapeutische optie geworden voor de behandeling van vele soorten kanker.
Het wereldwijde ontwikkelingsprogramma van nivolumab omvat een breed spectrum van klinische onderzoeken van alle fasen en verschillende soorten kanker. Tot op heden hebben meer dan 25.000 patiënten deelgenomen aan het klinische onderzoeksprogramma van nivolumab.
In juli 2014 was nivolumab de eerste goedgekeurde remmer van het immuuncontrolepunt PD-1. Het is momenteel geregistreerd in 60 landen. In oktober 2015 werd de eerste combinatietherapie van Bristol-Myers Squibb, nivolumab + ipilimumab, goedgekeurd voor de behandeling van gemetastaseerd melanoom en is nu goedgekeurd in meer dan 50 landen.
Informatie over hoofd-halskanker
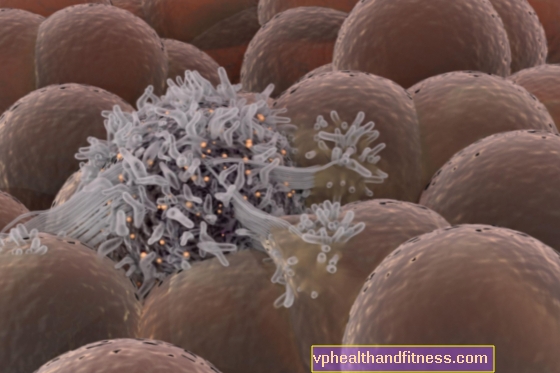
Kankers die bekend staan als hoofd- en nekkankers ontstaan meestal in de plaveiselepitheelcellen die de vochtige slijmvliesoppervlakken in het hoofd en de nek bedekken, zoals in de mond, neus en keel. Neoplasmata van het hoofd en de nek zijn de zevende meest voorkomende kanker ter wereld. Jaarlijks worden naar schatting 400.000 tot 600.000 nieuwe gevallen en 223.000 tot 300.000 sterfgevallen door deze oorzaak geschat. Overlevingspercentages na vijf jaar zijn minder dan 4% voor gemetastaseerde stadium IV-ziekte. Plaveiselcelcarcinoom van het hoofd-halsgebied (SCCHN) is verantwoordelijk voor ongeveer 90% van alle kankers in dit gebied. De wereldwijde incidentie van deze vorm van kanker zal tussen 2012 en 2022 met 17% toenemen. Risicofactoren voor plaveiselcelkanker van het hoofd-halsgebied zijn onder meer roken en alcoholgebruik. Infectie met het humaan papillomavirus (HPV) is ook een risicofactor die leidt tot een snelle toename van de incidentie van orofaryngeale plaveiselcelcarcinomen van het hoofd en de nek in Europa en Noord-Amerika. Bij plaveiselcelneoplasma's van het hoofd en de nek is de kwaliteit van leven van patiënten vaak verminderd als gevolg van verminderde fysiologische functies (ademen, slikken, eten, drinken), persoonlijke kenmerken (uiterlijk, spreken, stem), sensorische functies (geuren waarnemen, horen) en sociale en psychologische functies .






















---badanie-wydolnoci-y-i-ttnic.jpg)
