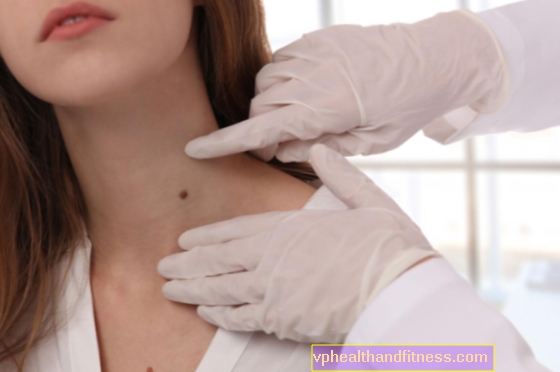
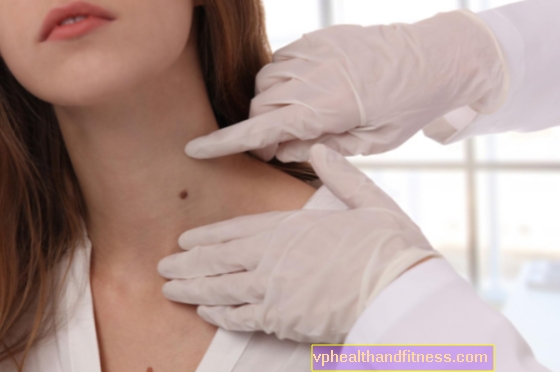
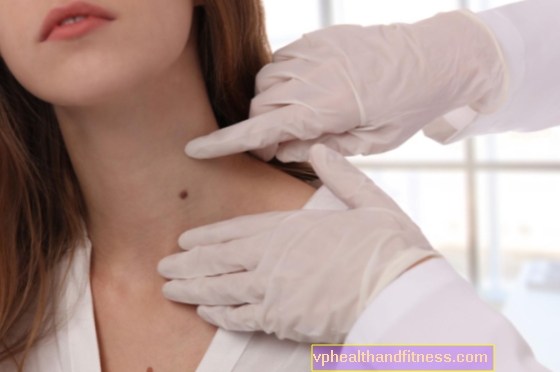
Elke blisterverpakking bevat 28 tabletten. oppervlak: 24 tabletten lichtroze, elk met 3 mg drospirenon en 0,02 mg ethinylestradiol; 4 tafels wit (placebo) dat geen werkzame stoffen bevat. Het medicijn bevat lactose.
| Naam | Inhoud van de verpakking | De werkzame stof | Prijs 100% | Laatst gewijzigd |
| YAZ | 28 stuks (24 stuks + 4 stuks), tafel pow. | Ethinylestradiol, Drospirenon | 63,61 PLN | 2019-04-05 |
Actie
Een monofasisch gecombineerd oraal anticonceptivum. Het basismechanisme van de anticonceptieve werking van het preparaat is de remming van de ovulatie en de inductie van veranderingen in het endometrium. Het 24-daagse regime laat een superieure onderdrukking van de follikelontwikkeling zien in vergelijking met het 21-daagse regime in een ovulatie-inhibitiestudie die gedurende 3 menstruatiecycli werd uitgevoerd. Bij therapeutische doses heeft drospirenon ook een anti-androgeen effect en een licht anti-mineralocorticoïde effect. Het heeft geen oestrogene, glucocorticoïde of antiglucocorticoïde eigenschappen (het farmacologische profiel van drospirenon lijkt sterk op dat van natuurlijk progesteron). Drospirenon wordt snel en bijna volledig geabsorbeerd na orale toediening en bereikt een Cmax na 1-2 uur De biologische beschikbaarheid is 76-85%, voedsel heeft geen invloed op de biologische beschikbaarheid. Bindt aan albumine, niet aan SGBH en CBG. Het wordt snel gemetaboliseerd; metabolieten worden uitgescheiden in de feces en urine. De T0,5 in de eliminatiefase is ongeveer 40 uur Ethinylestradiol wordt snel en volledig geabsorbeerd na orale toediening en bereikt de Cmax na 1-2 uur. Het is onderhevig aan een first-pass-effect dat wordt gekenmerkt door een grote interindividuele variabiliteit. De biologische beschikbaarheid is ongeveer 60%. Het is voor 98% gebonden aan plasma-eiwitten en induceert de hepatische synthese van SHBG en CBG. Het wordt volledig gemetaboliseerd, metabolieten worden uitgescheiden in gal en urine. T0,5 in de eliminatiefase is ongeveer 20 uur.
Dosering
Oraal: neem de tabletten in de volgorde die staat aangegeven op de verpakking, elke dag op ongeveer hetzelfde tijdstip van de dag, zo nodig met wat vloeistof. U dient 1 tablet in te nemen. dagelijks gedurende 28 opeenvolgende dagen: 24 roze tabletten, daarna 4 witte tabletten. Elke volgende verpakking moet worden gestart op de dag na inname van de laatste witte tablet van de vorige verpakking. De onttrekkingsbloeding begint gewoonlijk 2-3 dagen na het starten van de placebotabletten en is mogelijk niet volledig tegen de tijd dat met de volgende strip wordt begonnen. Begin met het gebruik van de voorbereiding. Als de patiënte de afgelopen maand geen hormonale anticonceptiemethode heeft gebruikt, moet de behandeling worden gestart op dag 1 van de cyclus (d.w.z. dag 1 van haar menstruatie). Als de patiënt eerder een ander gecombineerd oraal anticonceptivum heeft gebruikt, moet het innemen van tabletten de dag na inname van de laatste actieve tablet van het vorige gecombineerde anticonceptivum beginnen, maar niet later dan de dag na het einde van de pauze of na inname van de placebotabletten van het vorige gecombineerde anticonceptivum. Als een patiënt een therapeutisch vaginaal toedieningssysteem of een transdermale pleister gebruikt, dient het gebruik bij voorkeur te worden gestart op de dag van verwijdering, maar niet later dan de dag waarop de volgende pleister moet worden gebruikt. Als de patiënt eerder een anticonceptiemiddel met alleen progestageen heeft gebruikt (minipil, injectie, implantaat of intra-uterien systeem dat progestageen afgeeft), kan de bereiding in plaats van de minipil worden gestart op elke dag van de cyclus, voor het implantaat en het systeem - op de dag van verwijdering van het implantaat of systeem, voor injectie - op de dag waarop de volgende injectie zou worden gegeven; in al deze gevallen moet tijdens de eerste 7 dagen na inname van het preparaat een barrièremethode voor anticonceptie worden gebruikt. Bij een miskraam in het eerste trimester van de zwangerschap kan direct met de voorbereiding worden begonnen; het is niet nodig om andere anticonceptiemethoden te gebruiken. In het geval van een bevalling of een miskraam in het tweede trimester van de zwangerschap, mag de voorbereiding 21-28 dagen na de bevalling of na een miskraam worden gestart; als de patiënt later begint, moet gedurende de eerste 7 dagen een aanvullende anticonceptiemethode worden gebruikt. Bij patiënten die geslachtsgemeenschap hebben gehad na de bevalling of een miskraam hebben gehad alvorens het preparaat te gebruiken, moet zwangerschap worden uitgesloten of moet worden gewacht tot de eerste menstruatie optreedt. Behandeling van vergeten tabletten. Als u een witte tablet heeft overgeslagen, dient u dit te negeren aangezien dit placebotabletten zijn. Het moet echter uit de blisterverpakking worden verwijderd om een onbedoelde verlenging van de placebotabletfase te voorkomen. De hieronder beschreven informatie is alleen van toepassing in het geval van het weglaten van tabletten die werkzame stoffen bevatten - tabel roze. Als er minder dan 24 uur zijn verstreken sinds het vergeten van een tablet, blijft de anticonceptiebescherming behouden; Neem de gemiste tablet in zodra u eraan denkt en neem de volgende tablet op het gebruikelijke tijdstip in. Als er meer dan 24 uur zijn verstreken sinds het vergeten van een tablet, kan de werkzaamheid verminderd zijn, ga verder zoals hieronder beschreven. De aanbevolen tabletvrije periode is 4 dagen; het innemen van tabletten mag nooit langer dan 7 dagen onderbroken worden. 7 dagen ononderbroken tabletinname is vereist om een adequate onderdrukking van de hypothalamus-hypofyse-ovarium-as te behouden. Als u in week 1 (dag 1 tot 7) een tablet bent vergeten, neem deze dan zo snel mogelijk in, zelfs als dit betekent dat u twee tabletten tegelijkertijd moet innemen, en neem de volgende tabletten op het gebruikelijke tijdstip. De komende 7 dagen moet een barrièremethode voor anticonceptie worden gebruikt. Als u in de 7 dagen voorafgaand aan de vergeten tablet geslachtsgemeenschap heeft gehad, kunt u zwanger worden. Hoe meer tabletten er worden vergeten en hoe minder tijd er is verstreken sinds de placebotabletperiode, hoe groter de kans op zwangerschap. Als u de tablet in week 2 (dag 8 tot 14) bent vergeten, neem de tablet dan zo snel mogelijk in, zelfs als dit betekent dat u twee tabletten tegelijkertijd moet innemen, en neem de volgende tabletten op het gebruikelijke tijdstip. Mits de tabletten correct zijn ingenomen in de 7 dagen voorafgaand aan de eerste vergeten tablet, is het niet nodig om aanvullende anticonceptiemaatregelen te nemen. Als er echter meer dan 1 tablet is overgeslagen, moeten gedurende 7 dagen aanvullende barrièremethoden worden gebruikt. Als de tablet in de derde week (dag 15 tot 24) wordt overgeslagen, zijn er twee opties. Als het preparaat correct is gebruikt in de 7 dagen voorafgaand aan de gemiste tablet, kan een van de volgende aanbevelingen worden gekozen zonder de noodzaak om aanvullende anticonceptiemaatregelen te nemen; gebruik anders aanbeveling A en gebruik barrièremethoden voor anticonceptie gedurende 7 dagen. A - Neem de vergeten tablet zo snel mogelijk in, zelfs als dit betekent dat u twee tabletten tegelijk moet innemen, neem de volgende tabletten op het gebruikelijke tijdstip in totdat de werkzame tabletten op zijn. Gooi 4 witte (placebo) tabletten uit de laatste rij weg en begin meteen met het innemen van de tabletten uit de volgende strip (aan het einde van de tweede strip zal er een onttrekkingsbloeding optreden, u kunt last krijgen van spotting of doorbraakbloeding tijdens het innemen van de tabletten). B - De huidige verpakking kan worden stopgezet, de laatste rij placebotabletten mag tot 4 dagen worden stopgezet, inclusief de dagen dat de tabletten zijn overgeslagen, en daarna opnieuw worden gestart met een nieuwe verpakking. Advies bij ernstige gastro-intestinale stoornissen (braken, diarree). In dat geval is het mogelijk dat de opname van de werkzame stoffen niet volledig is en dienen aanvullende anticonceptiemaatregelen te worden genomen. Indien braken optreedt binnen 3 tot 4 uur na inname van een tablet, dient zo snel mogelijk een (extra) tablet te worden ingenomen. De extra tablet moet binnen 24 uur na de gebruikelijke dosis worden ingenomen. Als de patiënt het gebruikelijke doseringsschema niet wil veranderen, moet een extra tablet uit de volgende strip worden ingenomen. Als er> 24 uur zijn verstreken, volg dan de instructies voor het vergeten van tabletten. Beheer om het bloeden uit te stellen of te verzetten. Om een onttrekkingsbloeding uit te stellen, dient u de placebotabletten over te slaan en met de volgende strip te beginnen. De vertraging van de bloeding kan worden verlengd door meer tabletten in te nemen, zelfs tot het einde van de tweede strip. In deze verlengde cyclus kan een lichte doorbraakbloeding of spotting optreden. Daarna, na de placebotabletperiode, moet de bereiding worden hervat. Als u uw onttrekkingsbloeding wilt uitstellen tot een andere dag van de week, verkort dan de innameperiode van de placebotablet met het aantal dagen dat u de bloeding wilt uitstellen. Hoe korter het interval, hoe groter de kans dat er geen onttrekkingsbloeding zal optreden en dat er bij de volgende strip weinig doorbraakbloeding of spotting zal optreden.
Indicaties
Orale anticonceptie.
Contra-indicaties
Overgevoeligheid voor de werkzame stoffen of voor één van de hulpstoffen Aanwezigheid van of risico op veneuze trombo-embolie: veneuze trombo-embolie - actief (behandeld met anticoagulantia) of een voorgeschiedenis van veneuze trombo-embolie, bijv. Diepe veneuze trombose, longembolie; bekende erfelijke of verworven predispositie voor veneuze trombo-embolie, bijv. resistentie tegen geactiveerd proteïne C (inclusief factor V Leiden), antitrombine III-deficiëntie, proteïne C-deficiëntie, proteïne S-deficiëntie; uitgebreide chirurgie geassocieerd met langdurige immobilisatie; hoog risico op veneuze trombo-embolie vanwege meerdere risicofactoren. Aanwezigheid van of risico op arteriële trombo-embolie: arteriële trombo-embolie - actieve (bv. Myocardinfarct) of prodromale symptomen (bv. Angina pectoris; cerebrovasculaire ziekte - actieve beroerte, voorgeschiedenis van beroerte of voorgeschiedenis van prodromale symptomen (bv. Voorbijgaand) voorbijgaande ischemische aanval (TIA); bevestigde erfelijke of verworven neiging tot het optreden van arteriële trombo-embolische stoornissen, bijv. hyperhomocysteïnemie en de aanwezigheid van antifosfolipide-antilichamen (anti-cardiolipine-antilichamen, lupus-anticoagulans); migraine met focale neurologische symptomen; hoog risico op neurologische aandoeningen trombo-embolie als gevolg van meerdere risicofactoren of de aanwezigheid van een van de ernstige risicofactoren zoals: diabetes mellitus met vasculaire complicaties, ernstige hypertensie, ernstige dyslipoproteïnemie Huidige of eerdere ernstige leverziekte (totdat functionele tests terugkeren lever tot normale waarden). Ernstig of acuut nierfalen. Huidige of voorgeschiedenis van goedaardige of kwaadaardige levertumoren. Aanwezigheid of vermoeden van maligne neoplasmata die afhankelijk zijn van geslachtshormonen (bijv. Tumoren van de geslachtsorganen of de borsten). Bloeden uit het geslachtsorgaan met onbekende etiologie.
Voorzorgsmaatregelen
Voordat met het gebruik van het preparaat wordt begonnen (of voordat het opnieuw wordt gebruikt na de pauze), moet zwangerschap worden uitgesloten, moet een volledige medische geschiedenis (inclusief familiegeschiedenis), bloeddrukmeting en lichamelijk onderzoek worden uitgevoerd om contra-indicaties en aandoeningen die speciale zorg vereisen uit te sluiten. Tijdens het gebruik van het preparaat moeten controletests regelmatig worden herhaald, in overeenstemming met de toepasselijke richtlijnen. Als onregelmatige menstruatiebloedingen aanhouden of optreden bij een vrouw die eerder een regelmatige menstruatiecyclus heeft gehad, moet niet-hormonale etiologie worden overwogen en moet een passende evaluatie worden uitgevoerd om maligniteiten of zwangerschap uit te sluiten. Bijzondere voorzichtigheid is geboden (baten-risicobeoordeling) bij vrouwen met factoren die het risico op veneuze of arteriële trombo-embolie verhogen, waaronder: leeftijd (risico neemt toe met de leeftijd), positieve familiegeschiedenis, puerperium, langdurige immobilisatie, operatie , chirurgie van de onderste ledematen of ernstige verwondingen (het wordt aanbevolen om het preparaat ten minste 4 weken voor de geplande procedure stop te zetten en het pas 2 weken na terugkeer naar volledige mobiliteit opnieuw te gebruiken; als het preparaat niet van tevoren wordt stopgezet, moet een antistollingsbehandeling worden overwogen), obesitas (body mass index> 30 kg / m2), roken, dyslipoproteïnemie, hypertensie, migraine, hartklepafwijkingen, atriumfibrilleren. Er zijn discrepanties in de rol van spataderen en oppervlakkige tromboflebitis in de beginfase of progressie van veneuze trombose. De aanwezigheid van een ernstige of meerdere risicofactoren voor veneuze of arteriële aandoeningen kan een contra-indicatie zijn voor het gebruik van het preparaat.In dergelijke gevallen moet anticoagulantia worden overwogen. Voorzichtigheid is ook geboden bij aanwezigheid van andere ziekten die leiden tot stoornissen in de bloedsomloop, zoals diabetes mellitus, systemische lupus erythematosus, hemolytisch-uremisch syndroom, chronische inflammatoire darmziekte en sikkelcelanemie. Vanwege het risico op pancreatitis met voorzichtigheid gebruiken bij patiënten met hypertriglyceridemie of een positieve familiegeschiedenis van hypertriglyceridemie. Wees voorzichtig bij patiënten met: erfelijk angio-oedeem, endogene depressie, epilepsie, de ziekte van Crohn, colitis ulcerosa, geelzucht en / of pruritus geassocieerd met cholestase, cholelithiase, porfyrie, systemische lupus erythematosus, hemolithisch uremisch syndroom, sydolithisch uremisch syndroom , herpes tijdens de zwangerschap, otosclerose-gerelateerd gehoorverlies, aangezien deze ziekten kunnen worden verergerd door hormonale anticonceptiva. Bij patiënten met nierinsufficiëntie of bij wie de kaliumspiegels vóór aanvang van de behandeling in de bovengrens van het normale bereik lagen, vooral in het geval van gelijktijdig gebruik van kaliumsparende diuretica, wordt aanbevolen de kaliumspiegel tijdens de eerste behandelingscyclus te controleren. Diabetespatiënten moeten zorgvuldig worden gecontroleerd, vooral tijdens de eerste periode van gebruik van het preparaat, vanwege het risico van invloed van het geneesmiddel op de perifere insulineresistentie en glucosetolerantie. Vrouwen met neiging tot chloasma dienen blootstelling aan zonlicht of UV-straling te vermijden tijdens het gebruik van het preparaat. Het preparaat moet worden stopgezet in geval van vermoedelijke of gediagnosticeerde trombose, verhoogde frequentie of verergering van migrainepijn, acute of chronische leverdisfunctie (totdat de leverfunctieparameters weer normaal worden), terugkerende cholestatische geelzucht en / of jeuk geassocieerd met cholestase. In het geval van klinisch significante hypertensie tijdens het gebruik van het preparaat of hypertensie die niet reageert op farmacologische behandeling, moet het preparaat worden bewaard; in gerechtvaardigde gevallen kan het preparaat opnieuw worden gebruikt wanneer antihypertensieve therapie leidt tot normalisatie van de drukwaarde. Als er ernstige pijn in de bovenbuik, leververgroting of tekenen van intra-abdominale bloeding optreden, moet bij de differentiële diagnose rekening worden gehouden met de mogelijkheid van een levertumor. Patiënten met zeldzame erfelijke lactose-intolerantie, Lapp lactasedeficiëntie, glucose-galactose malabsorptie en die een lactosevrij dieet volgen, dienen rekening te houden met het lactosegehalte van het preparaat.
Ongewenste activiteit
Vaak: stemmingswisselingen, hoofdpijn, misselijkheid, pijnlijke borsten, baarmoederbloeding, amenorroe. Soms: depressie, nervositeit, slaperigheid, duizeligheid, paresthesie, migraine, spataderen, hypertensie, buikpijn, braken, dyspepsie, flatulentie, gastritis, diarree, acne, jeuk, huiduitslag, rugpijn, pijn in extremiteit, spierspasmen, vaginale candidiasis, bekkenpijn, borstvergroting, cysten in de borst, baarmoeder / vaginale bloeding, vaginale afscheiding, opvliegers, vaginitis, menstruatiestoornissen, dysmenorroe, oligomenorroe, menorragie, vaginale droogheid, abnormaal uitstrijkje van de baarmoederhals (Papanicolaou-methode), verminderd libido, zwakte, toegenomen zweten, oedeem (gegeneraliseerd oedeem, perifeer oedeem, gezichtsoedeem), gewichtstoename. Zelden: candidiasis, anemie, trombocytopenie, allergische reactie, endocriene stoornissen, verhoogde eetlust, anorexie, hyperkaliëmie, hyponatriëmie, anorgasmie, slapeloosheid, koude rillingen, conjunctivitis, droge ogen syndroom, oogziekte, tachycardie, flebitis, arteriële ziekte, bloeding loopneus, flauwvallen, vergrote buik, maag-darmstoornissen, vol gevoel in de maag en darmen, hiatale hernia, orale candidiasis, constipatie, droge mond, galblaaspijn, ontsteking van de galblaas, chloasma, eczeem (eczeem), alopecia, acneïforme dermatitis, droge huid, erythema nodosum, hirsutisme, huidaandoening, striae op de huid, contactdermatitis, lichtgevoelige dermatitis, huidknobbels, pijnlijke geslachtsgemeenschap, vulvovaginitis, bloeding na geslachtsgemeenschap, onttrekkingsbloeding, borstcyste, borstvergroting, borstkanker, cervicale poliep, atrofie van het baarmoederslijmvlies cyste, ovariumcyste, vergroting van de baarmoeder, malaise, gewichtsverlies. Niet bekend: overgevoeligheid, erythema multiforme. De volgende ernstige bijwerkingen zijn gemeld bij vrouwen die combinatie-OAC's gebruiken: veneuze en arteriële trombo-embolische aandoeningen (diepe veneuze trombose, longembolie, myocardinfarct, transiënte ischemische aanval; trombose in de hepatische, mesenteriale en mesenteriale aderen en slagaders is zeer zelden gemeld). nier-, cerebrale of retinale), hoge bloeddruk, acute of chronische leverdisfunctie, levertumoren (goedaardig, minder vaak kwaadaardig; deze kunnen leiden tot levensbedreigende intra-abdominale bloeding), chloasma. Bij vrouwen die inherent vatbaar zijn voor exogeen angio-oedeem, kunnen oestrogenen symptomen van angio-oedeem uitlokken of verergeren. Er zijn onduidelijke gegevens over het verband tussen combinatie-OAC's en de inductie of verergering van de volgende aandoeningen: de ziekte van Crohn, colitis ulcerosa, epilepsie, migraine, vleesbomen in de baarmoeder, porfyrie, systemische lupus erythematodes, zwangerschapsherpes, chorea van Sydenham, hemolytisch uremisch syndroom, cholestatische geelzucht. In verschillende epidemiologische onderzoeken is aangetoond dat baarmoederhalskanker bij langdurig gebruik van de pil een verhoogd risico loopt - het is niet bekend in hoeverre deze resultaten bijvoorbeeld worden beïnvloed door seksueel gedrag en door infectie met het humaan papillomavirus (HPV). Borstkanker wordt iets vaker gediagnosticeerd (de oorzaak-gevolg relatie met COC-gebruik is echter onbekend).
Zwangerschap en borstvoeding
Niet gebruiken tijdens zwangerschap. Gebruik het preparaat niet tot het einde van de borstvoeding (het medicijn kan de hoeveelheid verminderen en de samenstelling van voedsel veranderen; steroïde stoffen en hun metabolieten kunnen in de melk terechtkomen en de baby beïnvloeden).
Opmerkingen
Het gebruik van het preparaat kan de resultaten van laboratoriumtesten beïnvloeden, bijv. Biochemische parameters van de lever-, schildklier-, bijnier- en nierfunctie, concentraties van dragereiwitten (bijv. SHBH, lipoproteïnen), parameters van het koolhydraatmetabolisme, evenals coagulatie- en fibrinolyse-indices; veranderingen zijn over het algemeen binnen laboratoriumgrenzen. Drospirenon veroorzaakt een verhoging van de plasmarenine-activiteit en een verhoging van de aldosteronspiegels in het bloed.
Interacties
Geneesmiddelen die het levermetabolisme induceren (waaronder fenytoïne, barbituraten, primidon, carbamazepine, rifampicine, bosentan, ritonavir, nevirapine en mogelijk oxcarbazepine, topiramaat, felbamaat, griseofulvine en preparaten die sint-janskruid bevatten - kunnen het intermitterende bloedingseffect van Hypericum verzwakken). . Maximale enzyminductie vindt doorgaans plaats op dag 10, maar kan gedurende ten minste 4 weken na stopzetting van de behandeling aanhouden. Ook kunnen sommige antibiotica, zoals penicillines en tetracyclines, de effectiviteit van het preparaat verminderen. Vrouwen die een van de bovengenoemde korte termijn gebruiken geneesmiddelen (behalve rifampicine) dienen tijdelijk een aanvullend barrière-anticonceptiemiddel te gebruiken naast het gecombineerde orale anticonceptivum tijdens en gedurende 7 dagen na het einde van de combinatiebehandeling. Vrouwen die rifampicine gebruiken, moeten aanvullende anticonceptiemaatregelen nemen tijdens het gebruik van het antibioticum en gedurende 28 dagen na het stoppen ervan. Als de duur van de combinatietherapie ook het innemen van placebotabletten (witte tabletten) omvat, moeten de placebotabletten worden weggelaten en moet met de volgende strip worden begonnen nadat de laatste actieve tablet (roze tablet) van de vorige strip is ingenomen. Bij patiënten die langdurig met leverenzyminductoren worden behandeld, wordt een alternatieve, niet-hormonale anticonceptiemethode aanbevolen. Het preparaat kan de concentratie van ciclosporine verhogen en de concentratie van lamotrigine in het bloed en weefsels verlagen. Het risico van invloed van drospirenon op andere geneesmiddelen die door CYP-450 worden gemetaboliseerd, is laag, zoals in vitro en in vivo is bevestigd met behulp van de markersubstraten omeprazol, simvastatine en midazolam. Gelijktijdige toediening van drospirenon en ACE-remmers of NSAID's had geen significant effect op de bloedkaliumspiegels bij patiënten met een normale nierfunctie. De effecten van gelijktijdig gebruik met aldosteronantagonisten of kaliumsparende diuretica zijn echter niet onderzocht - in dit geval moeten de bloedkaliumspiegels tijdens de eerste behandelingscyclus worden gemeten.
Prijs
YAZ, prijs 100% PLN 63,61
Het preparaat bevat de stof: ethinylestradiol, drospirenon
Geneesmiddel vergoed: NEE